植物分子生理学
基幹講座
スタッフ
松下 智直
- 職位
- 教授
- 部屋
- 理学部2号館223号室
- Phone
- 075-753-4142
- Fax
- mat(at-mark)gr.bot.kyoto-u.ac.jp
嶋田 知生
- 職位
- 講師
- 部屋
- 理学部2号館221号室
- Phone
- 075-753-4140
- Fax
- tshimada(at-mark)gr.bot.kyoto-u.ac.jp
岡 義人
- 職位
- 助教
- 部屋
- 理学部2号館221号室
- Phone
- 075-753-4140
- Fax
- yoshitooka0302(at-mark)gmail.com
研究内容
本研究室では、植物が示す驚異的な環境適応能力の分子基盤として、環境刺激に応答したゲノム規模の遺伝子発現制御、およびその結果もたらされるプロテオームの多様化やタンパク質の細胞内局在変化・細胞内輸送、そして細胞・組織・器官間で行われる長距離シグナル伝達などの過程に着目し、それらの現象を遺伝子・タンパク質・細胞レベルで研究しています。その際、ゲノム科学、分子遺伝学、分子生物学、生化学、細胞生物学、植物生理学などの手法を複合的に駆使し、多面的なアプローチによって研究を展開しています。具体的な研究課題は以下の通りです。
1) 光環境情報による転写開始点制御
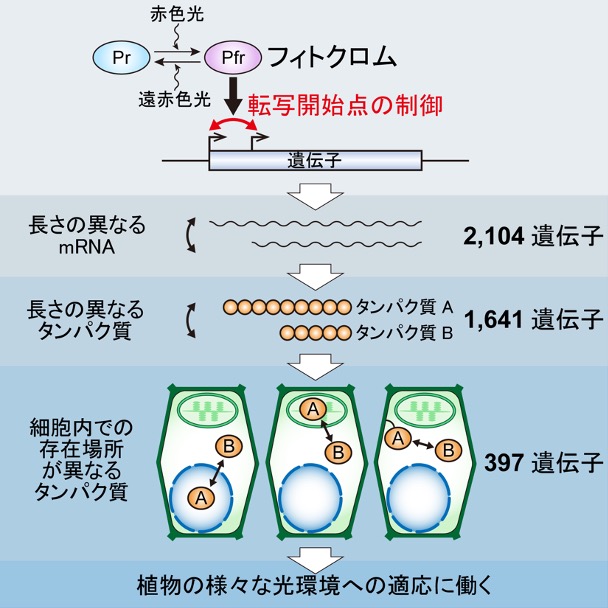
転写開始点選択とは、1つの遺伝子内に存在する複数の転写開始点から、長さの異なるmRNA分子が転写される現象のことです。私たちは最近、植物の光受容体であるフィトクロムが、シロイヌナズナにおいて2,000を超える遺伝子に直接働きかけそれらの転写開始点を変化させること、これに伴い約400のタンパク質の細胞内局在が光によって変化すること、そしてそれらタンパク質の細胞内局在変化が植物の様々な光環境への適応に寄与すること、などを発見しました(Ushijima et al., Cell 2017)(図1)。
これらの発見は、転写開始点選択という現象が、転写・スプライシング・翻訳と並び、真核生物のセントラルドグマにおける新たな普遍的一過程として、プロテオームの機能的な多様化に少なからず寄与することを強く示すものです。そして同規模の転写開始点変化は、フィトクロムシグナルに限らず、ありとあらゆるシグナルにより、真核生物において共通の分子機構で引き起こされるものである可能性が高いと考えられます。そこで私たちは、シロイヌナズナでのフィトクロムによる転写開始点制御をモデルケースとして、その分子機構を解明することで、真核生物に普遍的な新規遺伝子発現制御機構を明らかにし、セントラルドグマに新たな一過程を付け加えることを目指します。その結果として近い将来、生物の教科書の書きかえが行われるものと期待されます。
また、様々な環境刺激に応じて転写開始点が変化することで、同じ1つの遺伝子から、これまで知られていた機能とは全く異なる機能を持ったタンパク質が生じるケースが、次々と明らかになってきました。そこで今後私たちは、さらに多くの遺伝子について、転写開始点の切り替えによって発揮される遺伝子機能の多面性を明らかにし、多くの遺伝子が持つ「裏の顔」を暴くことで、プロテオームの未開領域の開拓を進めます。
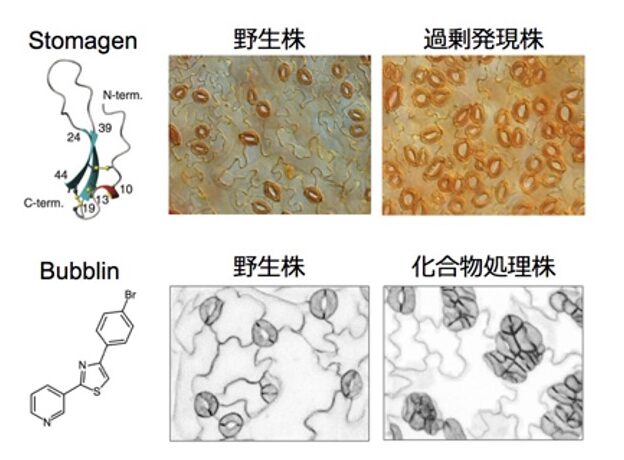
2) 葉の気孔ができるしくみの解明
気孔は葉の表面などに存在し、植物体と大気との間のガス交換に機能する大切な構造です。私たちはモデル植物シロイヌナズナを用いて、気孔がどのようなメカニズムで形成されているのかを調べています。私たちが発見したStomagenは45個のアミノ酸からなる生理活性ペプチドで、植物自身の遺伝子にコードされた内在性の因子です(Sugano et al., Nature 2010)(図2上)。Stomagenは雑草から作物や樹木に至る多種多様な植物がもっています。Stomagenは気孔前駆細胞に作用し、気孔(孔辺細胞)への細胞分化を促進する活性をもっています。Stomagenを植物に与えると気孔の数が増えることから、様々な植物のCO2吸収能力を上げる応用研究への発展も期待されます。
さらに私たちは最近、気孔形成に影響を与える新規化合物Bubblinを発見しました(図2下)。3,650種の低分子化合物からなるケミカルライブラリーをスクリーニングした結果、ピリジン-チアゾール化合物の一種が気孔の分布や形成パターンに影響を与えることを見出しました。私たちはこの化合物をBubblinと名付け解析を行いました。植物体にBubblinを処理すると、互いに隣接した気孔が多数形成されます。詳しい解析の結果、Bubblinは気孔前駆細胞の極性形成に影響しており、非対称分裂に異常を示すことが判明しました。植物細胞における極性形成メカニズムは未解明な部分も多く、今後Bubblinの解析によって気孔前駆細胞をモデルとした植物の細胞極性の形成をつかさどるメカニズムの解明につながることが期待されます。